Calciumsulfat (Gips)CaSO4 . 2H2O chemischer Nachweis des Mauersalzes
Frische, aber auch wieder durchfeuchtete, erhärtete Gipsmörtel enthalten gelöstes Sulfat, das Stahl zum Rosten bringt. Der pH-Wert einer Gipslösung liegt bei etwa 7. Für Rabitzarbeiten ist daher nur verzinktes Drahtgewebe zu verwenden. - Zink wird zwar auch durch Sulfatlösungen angegriffen, schützt aber das darunterliegende Eisen so lange, bis der Gipsputz trocken ist. Dann besteht bei Trockenheit allgemein keine Rostgefahr mehr.
Sulfattreiben
Bei der Zementherstellung werden zur Regulierung der Erstarrungszeit Gips oder Anhydrit zugegeben. (Auf die einzelnen Reaktionen wird hier nicht weiter eingegangen, siehe Hydration des Zementes )
Dringen später zum Beispiel aus dem Grundwasser oder Abwasser SO4-Ionen in den Beton mit seiner bereits verfestigten Gelstruktur ein, so kommt es zur Bildung von Ettringit mit erheblicher Kristallisationsdruck und Volumenexpansion, die den Zementstein zertreiben kann. Die Kräfte die zum Sulfattreiben führen, resultieren aus dem Kristallisationsdruck. Ettringit wird wegen seiner nadelförmigen, wirkenden Kristalle auch = Zementbazillus genannt. Die Kristallisationsdruckerhöhung wird auch auf die Bildung von Natriumsulfat, Brucit und Gips zurück geführt.
3 CaO*Al2O3*6H2O + 3CaSO4 + 26H2O --> 3CaO*Al2O3*CaSO4*32H2O (Ettringit)
Ist die Sulfatkonzentration sehr hoch, >1200 mg SO42-/l, so erfolgt auch folgende Reaktion
Ca(OH)2 + Na2SO4 + 2H2O --> CaSO4*2H2O + 2NaOH
Zusammenfassung der wesentlichen Kriterien zur Sulfatkorrosion:
- "Die Trisulfatbildung ist von der Wasserstoffionenkonzentration abhängig. Trisulfat entsteht im pH-Bereich von 10.8 bis 12.5. Bei pH-Werten > 12.5 entsteht Monosulfat.
- Die Beständigkeit des Trisulfates im Beton ist nicht nur vom pH-Wert abhängig, sondern auch von der Temperatur. Als Grenztemperaturen der Beständigkeit von Trisulfat werden in der Literatur Werte zwischen 40ºC und 70ºC angegeben.
- Die Temperaturbeständigkeit des Trisulfates hängt vom Einbau von Fremd-Ionen ab. Eisen-Ettringit wandelt sich bei geringen Temperaturen um.
- Zur Trisulfatbildung müssen Gips und 3 CaO*Al2O3 im stöchiometrischen Verhältnis vorliegen. Bei geringen Gipskonzentrationen bildet sich primär Trisulfat, dieses wird anschließend in Monosulfat umgewandelt.
- Greifen Carbonat-Ionen gemeinsam mit Sulfat-Ionen den Beton an, so können erstere bereits gebildete Trisulfate zerstören, da Calciumcarbonat die Phase mit dem geringsten Löslichkeitsprodukt ist. Sehr hohe Sulfatkonzentrationen führen zur Bildung von Gips statt Trisulfat.
- Die Eindringgeschwindigkeit aggressiver Lösungen in den Beton ist in starkem Maße von der Temperatur abhängig, sie kann sich zum Beispiel bei einem Temperaturanstieg von 15ºC auf 30ºC verdreifachen.[1]
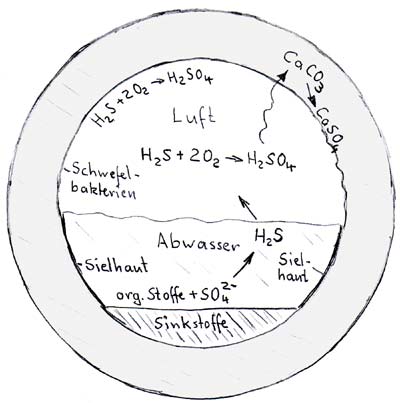
Beispiel für die chemischen Reaktionen in einem Abflussrohr
Nachweis
Nachweis als CaSO4 . 2H2O:
Die Bildung von Gipsnadeln ist ein spezifischer und empfindlicher Nachweis für Calcium. Die Fällung ist nicht quantitativ, da Calciumsulfat bei Zimmertemperatur in Wasser zu 1,5 * 10-2 Mol/l löslich ist.
1 Tropfen der HCl-sauren Lsg. Des CaCO3- beziehungsweise SrCO3-Niederschlag wird auf einem OT mit 1 Topfen 1 M H2SO4 vereinigt. Man lässt bei Zimmertemperatur langsam verdunsten und beobachtet nach etwa 10 Minuten unter dem Mikroskop (V:50-100) EG: 0,4 µg Ca pD 4,5.
Quellen:
[1] Schlüßler, Karl-Heinz; Mcedlov-Petrosjan, Ota Petrovich; Der Baustoff Beton, Grundlagen der Strukturbildung und der Technologie, 1990 Verlag für das Bauwesen Berlin, S. 79
Scholz, Wilhelm; Baustoffkenntnis, Werner-Verlag 13. Aufl. 1995, S.173
Weinmann, Kurt; Hösle, Richard; Handbuch Bautenschutz Bd 2, Bauphysik und Bauchemie, expert Verlag 1992, S.48
Jander, Gerhard; Blasius, Ewald; Lehrbuch der analytischen und präparativen anorganischen Chemie, S. Hinzel Verlag Leipzig 1965 S.197
Eigene Studienaufzeichnungen
© Altbausanierung | Baulexikon | Bauideen | Download | Impressum | Datenschutzerklärung | 3/2006 ![]()
